Dentro de los óxidos covalentes tenemos ejemplos en los que se forman pequeñas moléculas definidas, como ocurre con el dióxido de carbono CO2 cuya molécula consta de un átomo de carbono unido mediante enlaces covalentes dobles a dos átomos de oxígeno. Sin embargo, el óxido de silicio SiO2 (sílice) no forma moléculas sino estructuras cristalinas y polímeros a partir de celdas tetraédricas formadas por un átomo de silicio, que se sitúa en el centro del tetraedro, y 4 átomos de oxígeno situados en cada vértice del tetraedro. Entre el silicio y cada uno de los 4 oxígenos hay un enlace covalente simple, por lo que esta estructura tiene una carga negativa “-4”, es decir [SiO4]4-.
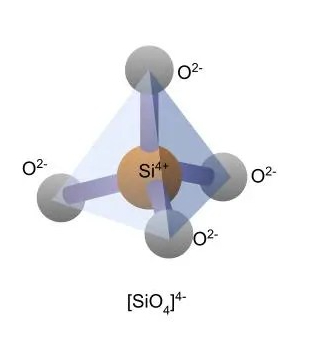
Los silicatos son todos aquellos minerales que tienen como unidad básica fundamental al tetraedro de silicio (SiO4) 4- , es decir, un catión de silicio (Si4+) enlazado con 4 aniones de oxígeno (O2-), los cuales se hallan dispuestos a su alrededor en las direcciones de los vértices de un tetraedro. Los silicatos nunca forman moléculas y debido a la carga descompensada del tetraedro base, se unen entre sí compartiendo oxígenos o bien a través de cationes. La sílice o el cuarzo es un silicato, pero también otros muchos compuestos formados con los tetraedros [SiO4]4-.
En general, los silicatos pueden definirse como compuestos formados por aniones que tienen la fórmula general [SiO4-x(4-2x)- ]n para 0 ≤ x ≤ 2
Las combinaciones que se obtienen considerando las distintas clases de uniones entre tetraedros (compartir oxígenos o enlazarse mediante cationes) y los diferentes cationes (monovalentes, divalentes, trivalentes o tetravalentes) determinan el tipo de silicato y sus características.
Además, en la red formada por los tetraedros [SiO4]4-, se suelen colar otros tetraedros formados por el aluminio porque el tetraedro de aluminio es muy similar en tamaño (radio iónico) y en carga eléctrica al tetraedro de silicio. Esos tetraedros de aluminio tienen la fórmula [AlO4]5- .
Los silicatos son, por tanto, estructuras ordenadas formando cristales con distintas formas (cadenas, láminas o estructuras en tres dimensiones). que se clasifican en los grupos o subclases siguientes:
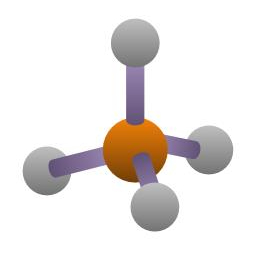
Ortosilicatos o Nesosilicatos
Se obtienen con el valor x=0 en la fórmula general y su fórmula es (SiO4)4-. Son silicatos con tetraedros sueltos unidos entre sí a través de cationes. No tienen oxígenos compartidos entre dos tetraedros. Dentro de esta subclase están: Zircón, Olivino, Granate, Topacio y Aluminosilicatos (Andalucita, Jadarita, Sillimanita, Distena).
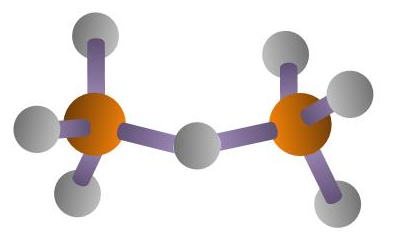
Sorosilicatos
Se obtienen con el valor x=0,5 en la fórmula general y su fórmula es [Si2O7]6-. Los tetraedros se unen de dos en dos por un vértice para formar los aniones. Los aniones formados por parejas de tetraedros se unen entre sí a través de cationes. En esta subclase están: Epidota, Melilita, Torveitita, Hemimorfita, Lawsonita
Ciclosilicatos
Se obtienen con el valor x=1 en la fórmula general. Los tetraedros se unen formando anillos compartiendo oxígenos entre sí. Hay anillos de tres, cuatro o seis tetraedros. Dependiendo del tamaño de los anillos sus fórmulas son [Si3O9]6- y [Si6O18]12- .
Se agrupan en: Turmalina y sus variedades (chorlo, dravita, indigolita, lidicoaíta, elbaita, rubelita), Berilo y sus variedades (esmeralda, morganita), Cordierita, Dioptasa.

Inosilicatos
Se obtienen con el valor x=1 en la fórmula general y están formados por grupos de tetraedros unidos en largas cadenas de longitud indefinida con fórmula [SiO3]2- . Los más comunes son los que presentan cadenas simples llamados piroxeno, mientras que los llamados anfíboles tienen cadenas dobles. Son fibrosos y se agrupan en: Piroxeno, Anfíbol, Piroxenoide y Anfiboloide.

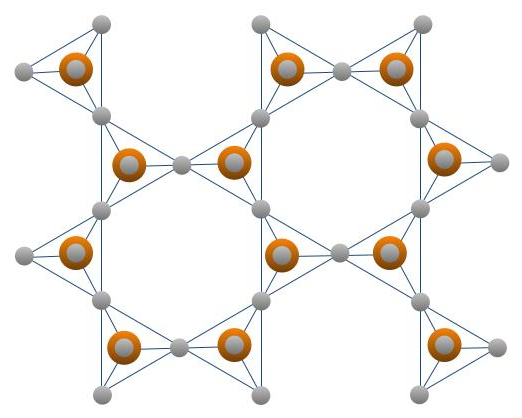
Filosilicatos
Se obtienen con el valor x=1,5 en la fórmula general de forma que se obtiene su fórmula [Si2O5]-2 . Son tetraedros unidos por tres vértices a otros, formando una red plana que se extiende en un plano de dimensiones indefinidas. Son de hábito foliado. Se agrupan en: Clorita, Micas, Talco, Pirofilita, Serpentinas y Caolinita.
Las arcillas están formadas por filosilicatos, sobre todo por Caolinita.
Tectosilicatos
Se obtienen con el valor x=2 en la fórmula general de forma que se obtiene su fórmula [SiO2] con carga neutra. Su estructura consiste en tetraedros unidos por sus cuatro vértices a otros tetraedros, produciendo una malla de extensión tridimensional, compleja (SiO2)n . Son tectosilicatos la sílice, es decir, el dióxido de silicio, pero también otros silicatos muy utilizados en cerámica como los feldespatos. La sustitución de silicio por aluminio en algunos tetraedros permite que en la malla se coloquen cationes. Se agrupan en: Cuarzo, Tridimita, Cristobalita, Feldespatos, Zeolita, Escapolita.
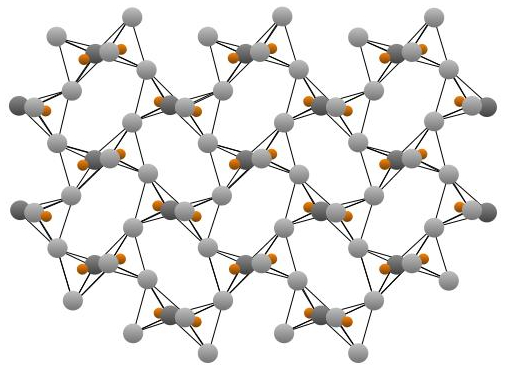
Silicatos con nombre propio
A muchos silicatos, de las subclases ortosilicatos/nesosilicatos e inosilicatos principalmente, se les denomina en muchas ocasiones con el nombre de los cationes con los que se enlazan, ya sea un catión mayoritario o los dos cationes más abundantes en la composición, y los silicatos más utilizados tienen además su propio nombre:
- Silicato de zinc o Willemita Zn2SiO4 es un ortosilicato de zinc.
- Silicato de zirconio o Zircón ZrO2·SiO2 es un ortosilicato utilizado como opacificante.
- Ortosilicatos de aluminio de fórmula Al2O3·SiO2 como la Sillimanita o andalucita, cianita y distena. Silicatos utilizados como fuente de alúmina.
- Titanita o esfena: Silicato de titanio y calcio de la subclase nesosilicatos. Su fórmula es CaTiSiO5 o bien, para mayor claridad CaO·TiO2·SiO2
- Esfena de Calcio y Estaño (con Cromo): Muy similar a la titanita, se trata de un nesosilicato de calcio y estaño con fórmula CaSnO(SiO4) a la que se añade cromo para formar pigmento rosa.
- Silicato de sodio o vidrio soluble: Na2SiO3. Es un inosilicato que se utiliza como defloculante y como aglutinante. Se suministra en líquido o en disolución concentrada que irrita y reseca la piel. Cuando se seca obtiene la apariencia de un cristal.
- Silicato de calcio o Wollastonita: CaO·SiO2 . Es un inosilicato piroxeno utilizado para introducir CaO en los vidriados.
- Silicato de magnesio o Enstatita MgO·SiO2 . Inosilicato piroxeno como materia prima de magnesio
- Diópsido: CaO·MgO·2SiO2 Inosilicato piroxeno de calcio y magnesio
- Espodúmeno Li2O·Al2O3·4SiO2 es un piroxeno de litio
Un comentario en “Silicatos”