Si aplicamos calor a un sólido cristalino (línea roja del gráfico siguiente) su volumen comenzará a hacerse más grande pero se mantendrá la estructura cristalina hasta llegar a la temperatura de fusión. En ese momento, el cristal ya no soporta la vibración que produce la absorción de calor y los enlaces se rompen, formándose un líquido. Hay un cambio radical de volumen ya que los líquidos siempre tienen mayor volumen que los sólidos.
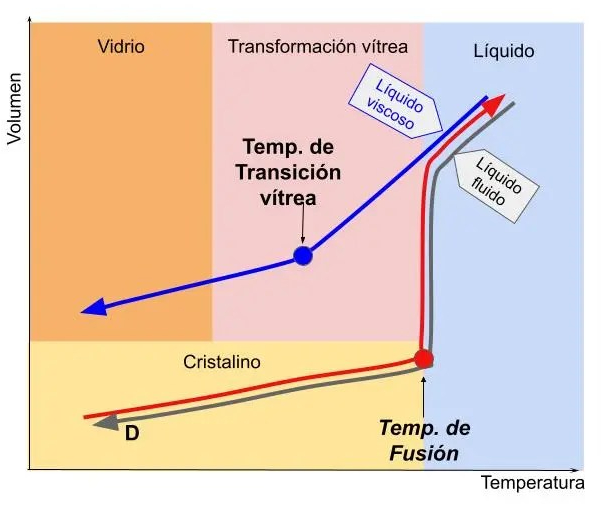
Si seguimos aumentando la temperatura, el líquido aumentará progresivamente su volumen.
Después comienza el enfriamiento, y en el gráfico se representan dos líneas de enfriamiento. La línea gris corresponde a materiales que tienen una viscosidad baja cuando están en estado líquido. La línea azul representa el comportamiento de materiales con alta viscosidad en estado líquido.
Al llegar a la temperatura de fusión, que es la misma que la temperatura de solidificación, el líquido fluido (la línea gris) sufre una reducción radical de volumen y se convierte de nuevo en un sólido cristalino. Un enfriamiento adicional da como resultado un cambio gradual de volumen con la formación de fases cristalinas a lo largo de la línea gris, a temperaturas por debajo de la temperatura de fusión y solidificación.
El líquido fundido con viscosidad alta, la línea azul en la gráfica, realiza un enfriamiento “rápido” con respecto al tiempo que necesitan los átomos para ordenarse en un cristal, de forma que el volumen se sigue reduciendo de forma progresiva más allá de la temperatura de solidificación. Esto significa que se evita la nucleación de cristales y su crecimiento. A medida que la masa fundida continúa enfriándose, la viscosidad también aumenta de modo que los átomos se quedan cada vez más estáticos formándose así una estructura vítrea.
La temperatura de transición vítrea corresponde a la temperatura a la que el líquido sobre-enfriado comienza a solidificar en forma vítrea.
El enfriamiento “rápido”, para que la transformación vítrea sea un éxito, se mide con la velocidad crítica de enfriamiento Rc, que es la rapidez con que un líquido debe ser enfriado para evitar las formaciones cristalinas. En el caso del silicio, Rc = 9·10-6 ºC/seg, lo que equivale a 0,03 ºC/hora, por lo que no parece fácil que un líquido fundido de sílice pueda cristalizar.
Para tener una idea de los valores de Rc, podemos decir que los metales fundidos cristalizan con Rc = 9·108 ºC/seg… o sea un metal forma cristales 1014 veces más rápido que el silicio.
La velocidad crítica de enfriamiento Rc depende de la viscosidad del líquido fundido. Es decir, cuando tenemos un vidriado fundido en el que se han mezclado sílice, boro, aluminio y diversos modificadores alcalinos o alcalinotérreos, tendremos un rango de temperaturas de fusión con distintas viscosidades, y la Rc será distinta para cada velocidad.
Las curvas TTT son curvas de Tiempo-Temperatura-Transformación y son una representación muy visual que permite saber el tiempo que tarda en transformarse un líquido en cristal en función de la temperatura. Se entiende por “cristal” a un volumen de red cristalina de 10-6 que es un tamaño que puede observarse.
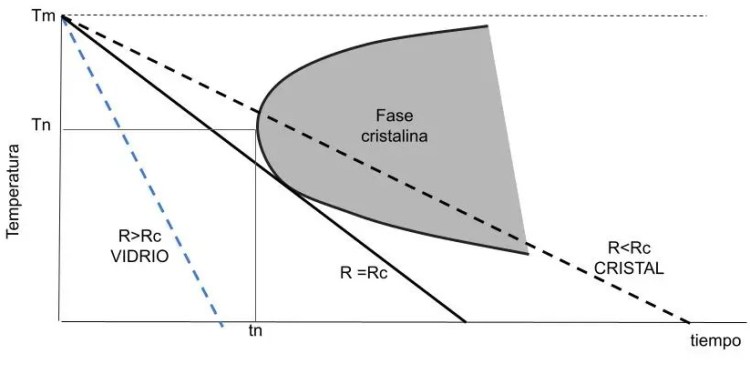
Estas curvas tienen forma de “C” o de “nariz” como se las conoce comúnmente. Representan la curva de cristalización de un material o mezcla de materiales. Si Tm es la temperatura de fusión de la mezcla, puede verse en la curva que a la temperatura Tn (K) aparecen cristales desde el instante tn (segundos), pero a temperaturas mayores o menores se necesita más tiempo para que aparezcan cristalizaciones. Esto es debido a que la fuerza termodinámica que hay que superar para que se produzca la cristalización aumenta cuando aumenta el super-enfriamiento , a la vez que disminuye la movilidad de los átomos.
La velocidad de enfriamiento se representa en este gráfico como una recta que va desde la temperatura de fusión Tm hasta la línea del tiempo, de forma que cuanto más inclinada sea esta recta menor será la velocidad de enfriamiento. La denominada velocidad crítica Rc es la recta que pasa tangente con la curva “C” de la mezcla. Y, como puede verse en el gráfico, una velocidad menor de enfriamiento R<Rc atraviesa la zona de cristalización de la “C”. Por el contrario, una velocidad superior de enfriamiento R>Rc produce un vidrio sin cristalizaciones ya que no atraviesa la “C”.
Cuanto más cercana está la nariz a la línea de ordenadas de temperaturas, tendremos un formador de red peor ya que la formación de cristales se producirá muy rápidamente. Podemos ver en la siguiente figura tres curvas “C” correspondientes a una mezcla cristalina (azul), una semicristalina (verde) y una mezcla vítrea (rojo) donde puede verse como la mezcla vítrea está mucho más separada de las ordenadas. En esta figura también vemos a la derecha una escala de viscosidad, que aumenta según baja la temperatura.
La mezcla cristalina (azul) tiene velocidad de enfriamiento crítica Rc muy alta y se sitúa va estará muy cerca en el tiempo a la temperatura Tm (temperatura de fusión) y la formación de cristales comenzará rápidamente.
El estado de líquido super enfriado de la mezcla vítrea necesita 104 segundos para alcanzar la estabilidad, es decir, para llegar a la temperatura de transición vítrea Tg.
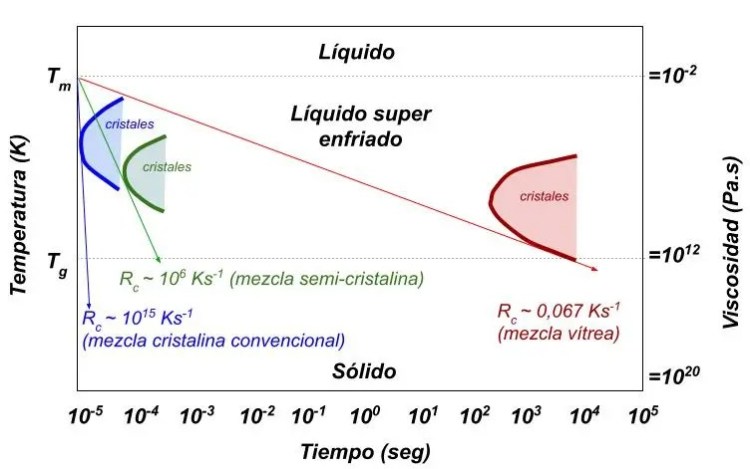
La velocidad crítica de enfriamiento Rc = 0,067 K seg-1 es un valor adecuado para la formación de estructuras vítreas, y esta velocidad es 108 (cien millones) veces más pequeña que la velocidad de enfriamiento de un compuesto amorfo.
Turnbull definió el “ratio de transición vítrea Trg” como la razón entre las temperaturas Tg (temperatura de transición vítrea) y Tm (temperatura de fusión), es decir: Trg = Tg/Tm.
De acuerdo con este ratio, un líquido con Trg ≥ 2/3 se vuelve muy lento para cristalizar y puede ser superenfriado para alcanzar un estado vítreo con una velocidad de enfriamiento baja. Este criterio sencillo es una forma de evaluar la posible cristalización de un líquido fundido.
En resumen, la formación de una estructura vítrea se produce cuando la velocidad crítica de enfriamiento Rc es lo suficientemente baja como para permitir realizar enfriamientos más rápidos. Y para disminuir Rc hay que aumentar la viscosidad.
En los vidriados cerámicos, la cantidad de alúmina en la mezcla aumenta mucho la viscosidad, por lo que podemos decir que la alúmina es el mayor inhibidor de la formación de cristales. Pero si lo que queremos es que se desarrollen cristales porque deseamos una superficie mate, o ciertos efectos especiales… buscaremos mezclas con una viscosidad menor.
La formación de cristales a partir del líquido fundido se inicia con la llamada nucleación y continúa con la fase de crecimiento. Tanto la nucleación como el crecimiento de cristales pueden ocurrir simultáneamente durante el enfriamiento.
La nucleación comienza con la agrupación de unos pocos átomos o iones que forman el núcleo del cristal. Para que esto ocurra no hace falta una gran difusión atómica sino fuerza termodinámica que impulse la nucleación.
Una vez formado un pequeño núcleo de cristal comienza el crecimiento. La formación de núcleos es muy grande pero suelen permanecer y crecer los núcleos más grandes, mientras que los núcleos pequeños tienden a disolverse de forma que sus átomos/iones ayudan al crecimiento de los más grandes. La fuerza termodinámica favorece la formación de los núcleos grandes.
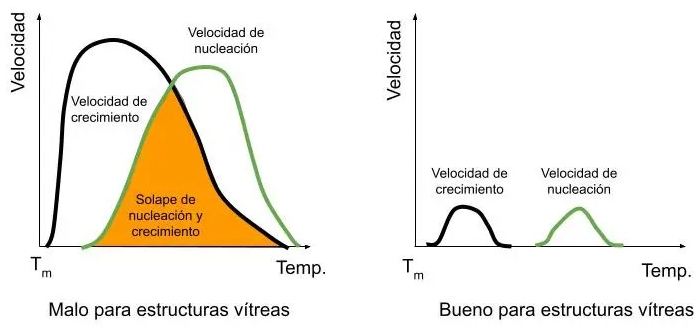
Dependiendo de los materiales, las temperaturas de nucleación y de crecimiento cristalino pueden solaparse o pueden producirse a distintas temperaturas. Cuando utilizamos formadores de red como la sílice, las curvas no se solapan, la nucleación comienza bastante por debajo de la temperatura de fusión y el crecimiento de los cristales es lento
Otros materiales que cristalizan más fácilmente comienzan la nucleación masiva a una temperatura muy cercana a Tm y el crecimiento de los cristales es muy rápido. Las curvas de nucleación y de crecimiento se solapan y son altas a las mismas temperaturas.
La velocidad de nucleación es función de la densidad de átomos, de la velocidad máxima a la que dichos átomos pueden moverse, de la probabilidad termodinámica de que surja una formación de un núcleo y de la probabilidad de difusión atómica.
La velocidad de crecimiento depende de la difusión atómica en la superficie del núcleo y de la capacidad de cristalización de la red expuesta.

Un comentario en “Cinética de la estructura vítrea”